| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Übergangselemente Übergangselemente  Zinkgruppe Zinkgruppe  Zink Zink  Zinkchlorid Zinkchlorid |
|||||||||||||||
| Siehe auch: Salzsäure, Zink, Chloride | |||||||||||||||






|
|||||||||||||||
ZinkchloridAutor: Hans Lohninger
Zinkchlorid kann durch Auflösen von Zink in Salzsäure dargestellt werden:
Zn + 2 HCl 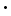 4 H2O. Erwärmt man eine Zinkchlorid-Lösung, so kristallisiert es in Form des Monohydrats, ZnCl2 4 H2O. Erwärmt man eine Zinkchlorid-Lösung, so kristallisiert es in Form des Monohydrats, ZnCl2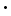 H2O. Wird das Monohydrat weiter erhitzt, verliert es das Kristallwasser zur Gänze; ein Teil des Zinkchlorids zersetzt sich dabei und bildet Zinkoxid: H2O. Wird das Monohydrat weiter erhitzt, verliert es das Kristallwasser zur Gänze; ein Teil des Zinkchlorids zersetzt sich dabei und bildet Zinkoxid:
ZnCl2 In der organischen Chemie wird Zinkchlorid (gelöst in konzentrierter Salzsäure) als Lucas-Reagens zur Unterscheidung von primären, sekundären und tertiären Alkoholen eingesetzt (primäre Alkohole reagieren nur in der Wärme, sekundäre langsam, und tertiäre schnell unter Bildung von Alkylchloriden. Zinkchlorid wird auch als Katalysator zur Chlormethylierung verwendet. Weiters wird es in Lötpasten und Lötwasser eingesetzt (siehe auch Lot und Löten). Zinkchlorid dient auch in Batterien als Elektrolyt. ZnCl2-Batterien sind eine Weiterentwicklung des Leclanché-Elements (Ersatz des Ammoniumchlorids als Elektrolyt durch Zinkchlorid). Zinkchloridbatterien haben eine bessere Kapazität die - belastungsabhängig - um fünf bis 35% höher ist (je höher die Belastung um so stäker die Kapazitätserhöhung).
Eine andere Anwendung ist die Erzeugung von künstlichem Nebel durch Nebelkerzen. Dabei wird feines Aluminiumpulver, Zinkoxid und Hexachlorethan zu Zinkchlorid umgesetzt, das dann aufgrund seiner hygroskopischen Wirkung Wasser aus der Luft aufnimmt und kleine Tröpfen bildet, die als Nebel erscheinen. Achtung, der Nebel ist ätzend und sollte nicht eingeatmet werden.
|
|||||||||||||||
Home  Übergangselemente Übergangselemente  Zinkgruppe Zinkgruppe  Zink Zink  Zinkchlorid Zinkchlorid |
|||||||||||||||
Last Update: 2013-08-08


 ZnCl2 + H2
ZnCl2 + H2