| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Übergangselemente Übergangselemente  Zinkgruppe Zinkgruppe  Zink Zink  elementares Zink elementares Zink |
|||||||||||||||||||||
| Siehe auch: Technische Darstellung von Zink, Periodensystem der Elemente, Cadmium, Zinkchlorid, Zinksulfid | |||||||||||||||||||||






|
|||||||||||||||||||||
ZinkAutor: H. Lohninger
GeschichteZink war bereits im Mittelalter bekannt, man wusste zu dieser Zeit allerdings noch nichts von chemischen Elementen. Messing (eine Zink-Kupfer-Legierung) war bereits im Altertum bekannt; man gewann es aus Zink- und Kupfererzgemischen. 1746 erkannte A.S. Marggraf, dass es sich bei Zink um ein chemisches Element handelt.VorkommenZink kommt in der Natur nur gebunden vor. Die wichtigsten Erze sind Sphalerit und Wurtzit (Zinkblende, Zinksulfid mit verschiedenen Kristallstrukturen), Smithonit (Zinkspat, Zinkcarbonat, ZnCO3) und Kieselzinkerz (Zn4(OH)2[Si2O7]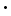 H2O). H2O).
EigenschaftenZink ist ein bläulich-weiß glänzendes Metall, das bei Raumtemperatur spröde ist. Im Temperaturbereich zwischen 100 und 150°C ist es aber formbar und kann zu Blechen gewalzt werden. Oberhalb von 200°C wird es wieder spröde, bis es bei 420°C schmilzt.
Zink steht in der elektrochemischen Spannungsreihe oberhalb von Eisen, weshalb ein verzinktes Eisen selbst dann nicht rostet, wenn die Zinkschicht verletzt wird (Ausbildung eines lokalen elektrochemischen Elements bei dem sich die unedlere Elektrode - das Zink - auflöst). Bei Weißblech (verzinntes Eisen) ist die Situation genau umgekehrt. Bei Verletzung der Zinnschicht rostet das darunter liegende Eisen um so schneller (hier löst sich das Eisen auf, da Zinn edler als Eisen ist). Zink ist ungift und ein essentielles Element (Tagesbedarf ca. 40 mg/kg Körpergewicht). Allerdings führt eine Überdosis an Zink (mehr als 1 Gramm) zu Übelkeit und Erbrechen. Säurehaltige Lebensmittel wie Fruchtsäfte oder mit Essig angerichtete Salate sollten daher nicht in verzinkten Gefäßen aufbewahrt werden. Darstellung und GewinnungDie Darstellung von Zink kann auf zwei Wegen erfolgen: zum einen durch Elektrolyse einer Zinksulfatlösung und zum anderen durch Reduktion von Zinkoxid durch Kohle. Geht man von Zinkblende (Zinksulfid) als Erz aus, so kann man das benötigte Zinkoxid durch Rösten erzeugen:
2 ZnS + 3 O2
ZnCO3 VerwendungZink wird in vielen Legierungen eingesetzt, wie z.B. Messing (70% Kupfer, 30% Zink) oder Prestal® (22% Aluminium, 78% Zink), das so fest wie Stahl aber trotzdem extrem dehnbar ist und sich darüberhinaus sehr gut gießen lässt. Etwa die Hälfte der Weltproduktion von Zink wird für das Verzinken von Eisenblech und Eisendraht verwendet, das dem Eisen den nötigen Korrosionsschutz gibt. Zink fungiert auch als negative Elektrode in verschiedenen Batterien: z.B. in der Zink-Kohle-Batterie, in Alkali-Batterien, in der Zink-Luft-Batterie oder in Quecksilber-Knopfzellen.
|
|||||||||||||||||||||
Home  Übergangselemente Übergangselemente  Zinkgruppe Zinkgruppe  Zink Zink  elementares Zink elementares Zink |
|||||||||||||||||||||
Last Update: 2013-08-08



 ZnO + SO2
ZnO + SO2