| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Varia Varia  Molmassenbestimmung Molmassenbestimmung |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||






|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
MolmassenbestimmungAutor: Hans Lohninger Da der Molmassenbestimmung durch Verdampfung (Molmasse = 22.4*Litermasse) naturgemäß - bedingt durch zu hohe Siedepunkte vieler Substanzen - Grenzen gesetzt sind, nützt man zur Bestimmung der Molmasse die Eigenschaft einer Lösung, einen gegenüber dem reinen Lösungsmittel erhöhten Siedepunkt bzw. einen erniedrigten Gefrierpunkt aufzuweisen. Eine elektrisch nicht leitende Lösung eines nicht flüchtigen Stoffes zeigt sowohl eine charakteristische Siedepunktserhöhung als auch eine charakteristische Gefrierpunktserniedrigung, deren Größe proportional zur molaren Konzentration ist und von der Art des Lösungsmittels, nicht aber von der Art des gelösten Stoffes abhängt (Raoult'sches Gesetz). Aus dem Raoult'schen Gesetz leiten sich die Grundlagen der Ebullioskopie (Molmassenbestimmung durch Siedepunktserhöhung) und Kryoskopie (Molmassenbestimmung durch Gefrierpunktserniedrigung) ab: Siedepunktserhöhung:
A = 1000
A = 1000 A .... Molmasse des gelösten Stoffes [g/mol] Tabelle der kryoskopischen und ebullioskopischen Konstanten wichtiger Lösungmittel:
Der oben dargestellte Zusammenhang gilt nur für nicht-dissoziierende Lösungsmittel. Bei dissoziierenden Lösungsmitteln muss der Dissoziationsgrad α berücksichtigt werden:
ΔT = KK,E ΔT .... Temperaturänderung [K] Dissoziationsgrad α einiger wichtiger 1-normaler Säuren und Basen bei 18°C
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Home  Varia Varia  Molmassenbestimmung Molmassenbestimmung |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Last Update: 2013-08-08


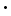 KE
KE