| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Übergangselemente Übergangselemente  Scandiumgruppe Scandiumgruppe  Lanthanoide Lanthanoide  Lutetium Lutetium |
|||||||
| Siehe auch: Periodensystem der Elemente, Ytterbium | |||||||






|
|||||||
LutetiumAutor: H. Lohninger
GeschichteLutetium wurde 1907 unabhängig voneinander von drei Forschern entdeckt: G. Urbain (Frankreich), C. Auer von Welsbach (Österreich) und C. James (USA). Alle drei isolierten Lutetium aus Ytterbiumoxid, das bis dahin als Reinstoff galt. Wie so oft bei nahezu gleichzeitigen Entdeckungen brach ein Streit um die Namensgebung aus, schließlich wurde der von G. Urbain vorgeschlagene Name "Lutecium"(1) akzeptiert, im deutschen Sprachraum wurde aber noch bis in die 1950er Jahre der Name "Cassiopium" verwendet. Vorkommen und GewinnungLutetium, das letzte Element in der Lanthanoidenreihe, kommt in geringen Mengen (1 bis 30 ppm) in Monazit vor. Es wird nach komplizierten Reinigungsschritten (Auflösen des Monazits in Schwefelsäure, Abtrennung der unlöslichen Oxalate, Glühen der Oxalate zu Oxiden, die in Salpetersäure gelöst werden; Abscheidung des unlöslichen Cernitrats; Lutetium wird dann zusammen mit anderen Seltenen Erden als Ammoniumnitrat-Doppelsalz abgeschieden) über Ionenaustauscher als reines Lutetiumchlorid, LuCl3, gewonnen. LuCl3 wird mit Calcium zu metallischem Lutetium reduziert.
EigenschaftenLutetium ist ein silbrig-weißes Metall das an Luft stabil ist und die höchste Dichte aller Lanthanoiden aufweist. Natürliches Lutetium besteht aus zwei Isotopen, das stabile Lu-175 (97.4%) und das radioaktive Lu-176 (2.6 %), das eine Halbwertszeit von 3.78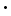 1010 Jahren aufweist. 1010 Jahren aufweist.
VerwendungLutetium hat aufgrund seines hohen Preises und der leichten Radioaktivität nur wenige Anwendungen gefunden. Vereinzelt wird es als Crack-Katalysator in der Petroleumindustrie verwendet. Weiters wird es in Spezialanwendungen eingesetzt, wie z.B. Cer-gedoptes Lutetiumsilikat als Detektor in der Positronen-Emissions-Tomographie (PET), oder als Dotierung für Magnetblasenspeicher. Lutetiumtantalat, LuTaO4, ist eine weiße Substanz mit der höchsten bekannten Dichte und wird deshalb für Röntgen-Phosphore eingesetzt.
|
|||||||
Home  Übergangselemente Übergangselemente  Scandiumgruppe Scandiumgruppe  Lanthanoide Lanthanoide  Lutetium Lutetium |
|||||||
Last Update: 2013-08-08


