| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Borgruppe Borgruppe  Aluminium Aluminium  Aluminiumoxid Aluminiumoxid |
|||||||||
| Siehe auch: Aluminium | |||||||||






|
|||||||||
AluminiumoxidAutor: Hans Lohninger
Aluminiumoxid kommt in zwei Modifikationen vor: das in der Natur vorkommende, sehr harte, hexagonale α-Aluminiumoxid ("Korund"), und das weiche kubische γ-Aluminiumoxid ("aktive Tonerde"),(1) das beim Glühen bei 1200°C in das α-Aluminiumoxid übergeht. Al2O3 ist für die Korrosionsbeständigkeit von Aluminium an der Luft verantwortlich, da Aluminium beim Kontakt mit Luft eine dünne aber undurchdringliche Oxidschicht aufbaut. Aluminiumoxid ist ein elektrischer Isolator mit einer vergleichsweise (für Keramikmaterial) guten Wärmeleitfähigkeit (30 W m-1 K-1). Es wird deshalb auch als Isoliermaterial in der Leistungselektronik eingesetzt. Das Hauptanwendungsgebiet von Aluminiumoxid ist neben der Erzeugung von Schleifmitteln die Produktion von metallischem Aluminium. Die technische Herstellung von Aluminiumoxid geschieht hauptsächlich aus Bauxit, das eine Mischung verschiedener Aluminiummineralien (Hydrargillit, Al(OH)3, Böhmit, γ-AlO(OH) und Diaspore, α-AlO(OH)) und einigen Verunreinigungen wie Quarz, Silikate oder Eisenoxid ist. Bauxit wird zuerst durch den Bayer-Prozess gereinigt. Da Bauxit nur ungefähr 40 bis 50% Aluminiumoxid enthält, muss der Rest abgetrennt werden. Dazu wird Bauxit im Autoklaven bei 200°C und 7 bar Druck mit heißer Natronlauge erhitzt. Dabei geht das Aluminiumoxid als Aluminiumhydroxid in Lösung:
Al2O3 + 2 NaOH + 3 H2O Die anderen Komponenten von Bauxit bleiben ungelöst und werden abfiltriert; die Rückstände bilden üblicherweise einen roten Schlamm ("Rotschlamm"), der einige Entsorgungsprobleme bereitet, da er u.a. Arsen und Cadmium enthält.(2) Die abgetrennte Lösung wird nun abgekühlt, nochmals feinfiltriert und dann so stark verdünnt, dass Aluminiumhydroxid ausfällt. Das abgeschiedene Aluminiumhydroxid wird zum Schluss auf 1050°C erhitzt, so dass es sich in Aluminiumoxid und Wasser zersetzt:
2 Al(OH)3
|
|||||||||
Home  Borgruppe Borgruppe  Aluminium Aluminium  Aluminiumoxid Aluminiumoxid |
|||||||||
Last Update: 2013-08-08



 2 Na[Al(OH)4]
2 Na[Al(OH)4]
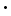 11 Al2O3
11 Al2O3