| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Übergangselemente Übergangselemente  Mangangruppe Mangangruppe  Rhenium Rhenium |
|||
| Siehe auch: Periodensystem der Elemente, Technetium, Bohrium | |||






|
|||
RheniumAutor: H. Lohninger
GeschichteDas Element Rhenium war wie Technetium bis 1920 unbekannt, man schloss nur aus dem Periodensystem, dass in der Mangangruppe 2 Elemente fehlten. Da Rhenium in Manganerzen praktisch nicht vorkommt, wurde es lange Zeit nicht entdeckt. Erst als W. Noddack, I. Tacke und O. Berg Platinerz und Columbit analysierten fanden sie 1925 Spuren des Elements 75. Später, 1928, konnten sie durch Aufarbeitung von 660 kg Molybdänit ein Gramm Rhenium gewinnen. 1929 wurde das Element 75 offiziell als neues chemisches Element anerkannt und ihm der Name Rhenium und das chemische Symbol Re zugewiesen.Vorkommen und HerstellungRhenium kommt in der Natur nur gebunden und in sehr geringen Konzentrationen vor. Rhenium-haltige Mineralien sind Molydänglanz, MoS2, Columbit, (Fe,Mn)[NbO3]2, und Gadolinit, Y2(Fe,Mn)Be2O2[SiO4]2. In allen Mineralien ist aber der Gehalt an Rhenium maximal etwa 10 bis 20 ppm, meist deutlich unter 1 ppm.
Die Weltproduktion von Rhenium beträgt ca. 25000 kg/Jahr. Die Weltreserven werden auf rund 10000 Tonnen geschätzt. EigenschaftenRhenium ist ein silbrig weißes hartes Schwermetall, das einen sehr hohen Schmelz- und Siedepunkt aufweist. Rhenium lässt sich gut schmieden und schweißen. Rhenium reagiert ab 400°C mit dem Luftsauerstoff unter Bildung von Re2O7. Ebenso reagiert es mit Schwefel und den Halogenen. Gegen nichtoxidierende Säuren ist Rhenium stabil, oxidierende Säuren lösen es auf. Rhenium bildet ähnlich wie Mangan Verbindungen auf allen Oxidationsstufen von -3 bis +7. Rheniumverbindungen mit hoher Oxidationsstufe sind stabiler als solche mit niedriger.
Rhenium kommt in der Natur mit zwei Isotopen vor: 185Re (37.4%) und 187Re (62.6%). Obwohl 187Re schwach radioaktiv ist (Halbwertszeit 4.12 VerwendungRhenium wird für Glühfäden in Vakuummessgeräten (Ionisationsmanometer) und in Massenspektrometern (Ionenquelle) eingesetzt. Weiters wird Rhenium in Hochtemperaturthermoelementen eingesetzt (W-Re kann bei Temperaturen von bis zu 2200°C verwendet werden). Der Einsatz von Rhenium als Katalysator in der Erdölindustrie ist rückläufig, da inzwischen preislich günstigere Alternativen gefunden wurden.Mengenmäßig den Hauptanteil macht aber die Verwendung von Rhenium in Legierungen für die Flugzeug- und Raumfahrtindustrie aus. So werden die Turbinenschaufeln von Jet-Triebwerken aus Legierungen mit einem Anteil von 3-6% Re gefertigt. Rhenium verleiht diesen Legierungen sehr gute mechanische Stabilität bei hohen Temperaturen.
Die Brennkammern von Raketentriebwerken werden mit Verbundstrukturen aus Iridium/Rhenium gefertigt, bzw. neuerdings aus Iridium/Rhenium/Kohlenstoff. Beim zweiten Ansatz dient der Kohlenstoff als strukturelle Hülle, Iridium als Oberfläche in der Brennkammer. Rhenium wird als Verbindungselement zwischen Iridium und Kohlenstoff in einer Schickdicke von ca. 0.5 mm aufgebracht (durch CVD - "chemical vapour deposition").
|
|||
Home  Übergangselemente Übergangselemente  Mangangruppe Mangangruppe  Rhenium Rhenium |
|||
Last Update: 2013-08-08



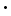 1010 Jahre), kommt es in der Natur häufiger vor als das stabile Isotop 185Re.
1010 Jahre), kommt es in der Natur häufiger vor als das stabile Isotop 185Re.