| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Übergangselemente Übergangselemente  Eisengruppe Eisengruppe  Eisen Eisen  Eisensulfide Eisensulfide |
|||||||||||||||||||||||
| Siehe auch: Eisen, Schwefelwasserstoff | |||||||||||||||||||||||






|
|||||||||||||||||||||||
EisensulfideAutor: Hans Lohninger Eisen bildet vier verschiedene Sulfide: Eisensulfid, FeS, Eisendisulfid, FeS2 (Pyrit, (kubisch), Markasit (orthorhombisch)), Dieisentrisulfid, Fe2S3, und Trieisentetrasulfid, Fe3S4 (Greigit). In den ersten beiden Sulfiden liegt das Eisen zweiwertig vor, im dritten dreiwertig, und im letzten zwei- und dreiwertig.
Eisensulfid, FeS: Eisensulfid ist eine hellbraune Substanz, die aber als technisches Produkt durch nicht umgesetzte Eisenreste meistens schwarz ist. FeS ist in Wasser unlöslich, mit Salzsäure reagiert es unter Bildung von Schwefelwasserstoff (FeS wird im Kipp'schen Apparat zur H2S-Erzeugung verwendet). Kocht man Eier zu lange (15 Minuten und mehr), so färbt sich der Dotter grünlich, was auf die Bildung von Eisensulfid zurückzuführen ist.
Dieisentrisulfid, Fe2S3: Schwarze Substanz, die nur gekühlt haltbar ist. Bei Raumtemperatur zerfällt es in ein Gemisch aus Eisensulfid, FeS, und Schwefel. Dieisentrisulfid kann durch Zugabe einer gekühlten Natriumsulfidlösung zu einer ebenfalls gekühlten Eisen(III)chlorid-Lösung dargestellt werden. Dabei fällt ein schwarzer Niederschlag von Fe2S3 aus.
Trieisentetrasulfid, Eisen(II,III)sulfid, Fe3S4, FeS
|
|||||||||||||||||||||||
Home  Übergangselemente Übergangselemente  Eisengruppe Eisengruppe  Eisen Eisen  Eisensulfide Eisensulfide |
|||||||||||||||||||||||
Last Update: 2013-08-08



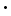 Fe2S3: Trieisentetrasulfid ist eine blau-schwarze Verbindung mit einem rosafarbenen Glanz. Es tritt in der Natur als das Mineral Greigit auf und ist ferromagnetisch. Trieisentetrasulfid wird von magnetotaktischen Bakterien dazu benutzt sich entlang des Erdmagnetfeldes auszurichten.
Fe2S3: Trieisentetrasulfid ist eine blau-schwarze Verbindung mit einem rosafarbenen Glanz. Es tritt in der Natur als das Mineral Greigit auf und ist ferromagnetisch. Trieisentetrasulfid wird von magnetotaktischen Bakterien dazu benutzt sich entlang des Erdmagnetfeldes auszurichten.