| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Kohlenstoffgruppe Kohlenstoffgruppe  Kohlenstoff Kohlenstoff  Kohlenmonoxid Kohlenmonoxid |
|||||||||||||||
| Siehe auch: Kohlendioxid, Phosgen | |||||||||||||||






|
|||||||||||||||
KohlenmonoxidAutor: Hans Lohninger
Kohlenmonoxid, CO, ist ein farbloses, brennbares, geruchloses, sehr giftiges Gas, das einerseits bei unvollständigen Verbrennungsvorgängen entsteht (Hausbrand, Autoabgase) und andererseits bei der Oxidation von Methan, das aus natürlichen Fäulnisprozessen stammt. Kohlenmonoxid verbrennt an der Luft mit bläulicher Flamme zu CO2. Es reagiert aber auch beim Erwärmen mit anderen Nichtmetallen wie Schwefel (unter Bildung von COS) oder Chlor (Phosgen, COCl2). Wichtig ist auch die katalytische Oxidation von CO im Autoabgas-Katalysator bei rund 400°C. Damit wird die Giftigkeit der Autoabgase entscheidend verringert (die Giftigkeit von CO beruht auf der Verdrängung von Sauerstoff im Hämoglobin durch Kohlenmonoxid). Kohlenmonoxid ist ein in der Industrie häufig eingesetztes Reduktionsmittel (z.B. für die Reduktion von Eisenerz, oder die Erzeugung von Wasserstoff durch Reduktion von Wasser). Kohlenmonoxid wird technisch entweder durch Umsetzung von Kohlenstoff mit Luft ("Generatorgas") hergestellt, oder durch Umsetzung von Kohlenstoff oder Methan mit Wasserdampf ("Wassergas", "Spaltgas", allgemein "Synthesegas"):
2 C + O2 + 4 N2 Boudouard-GleichgewichtKohlenmonoxid steht mit elementarem Kohlenstoff und Kohlendioxid gemäß folgender Reaktionsgleichung im Gleichgewicht:
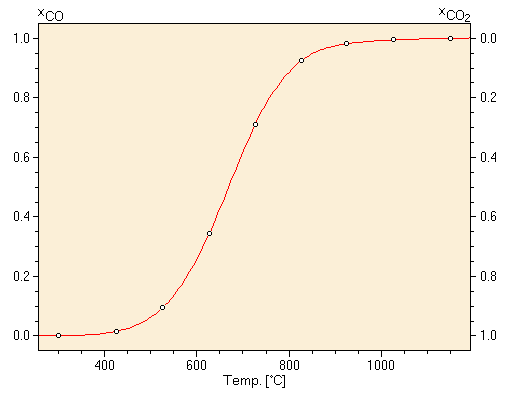
C + CO2 Diese Gleichgewichtsreaktion wird Boudouard-Gleichgewicht genannt (nach dem franz. Chemiker O.L. Boudouard) und hat in vielen industriellen Prozessen eine entscheidende Bedeutung (z.B. bei der Gewinnung von Eisen). Die Lage des Gleichgewichts hängt von der Temperatur und vom Druck ab. Bei höherer Temperatur und niedrigerem Druck verschiebt sich das Gleichgewicht nach rechts.
|
|||||||||||||||
Home  Kohlenstoffgruppe Kohlenstoffgruppe  Kohlenstoff Kohlenstoff  Kohlenmonoxid Kohlenmonoxid |
|||||||||||||||
Last Update: 2013-08-19


 2 CO + 4 N2 (Generatorgas)
2 CO + 4 N2 (Generatorgas) 2 CO
2 CO