| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Borgruppe Borgruppe  Aluminium Aluminium  Aluminiumchlorid Aluminiumchlorid |
|||||||||||||||
| Siehe auch: Aluminiumfluorid | |||||||||||||||






|
|||||||||||||||
AluminiumchloridAutor: Hans Lohninger
Wasserfreies Aluminiumtrichlorid, AlCl3, ist eine farblose Substanz, die sehr stark hygroskopisch ist und an feuchter Luft stark raucht. Die Rauchschwaden rühren von Chlorwasserstoff her, der durch Hydrolyse entsteht.
Wasserfreies Aluminiumchlorid wird technisch durch Chlorierung von Aluminium bei 800°C hergestellt. Kristallwasserhältiges Hexahydrat, AlCl3 Wasserfreies Aluminiumtrichlorid kann nicht durch Erhitzen des Hexahydrats gebildet werden, da dieses dabei hydrolysiert und Chlorwasserstoff abgibt:
AlCl3 Aluminiumchlorid liegt in der Schmelze und im gasförmigen Zustand bei niedrigen Temperaturen als Dimer, Al2Cl6, vor. Das ist auch der Grund dafür, warum sich das Volumen beim Schmelzen von Aluminiumchlorid um 85% erhöht und die elektrische Leitfähigkeit verschwindet. Bei steigender Temperatur zerfällt das Dimer in der Gasphase zunehmend in das Monomer, ab 800°C besteht der Dampf nur mehr aus Monomeren. Aluminiumtrichlorid weist eine adstringierende Wirkung auf. Die wässrige Lösung reagiert sauer und ist nicht stabil, da bedingt durch Hydrolyse Aluminiumhydroxid ausfällt. Eine Aluminiumchloridlösung kann nur durch Zugabe überschüssiger Salzsäure stabilisiert werden.
Aluminiumchlorid wird im Labor als Katalysator für Friedel-Crafts-Alkylierungen und -Acylierungen eingesetzt, weiters wird es als Flockungsmittel in der Wasseraufbereitung angewendet und von der Kosmetikindustrie als Antitranspirans (vor allem in Form von Polyaluminiumhydroxychlorid).
|
|||||||||||||||
Home  Borgruppe Borgruppe  Aluminium Aluminium  Aluminiumchlorid Aluminiumchlorid |
|||||||||||||||
Last Update: 2013-08-08


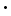 6H2O, kann durch Auflösen von
6H2O, kann durch Auflösen von  Al(OH)3 + 3 HCl + 3 H2O
Al(OH)3 + 3 HCl + 3 H2O