| Anorganische Chemie ist eine frei verfügbare Einführung in die anorganische Chemie. Details zum Buch finden Sie im Editorial.... |

|

Home  Chalkogene Chalkogene  Sauerstoff Sauerstoff  Ozon Ozon |
|||||||||||||||
| Siehe auch: Sauerstoff | |||||||||||||||






|
|||||||||||||||
OzonAutor: Hans Lohninger
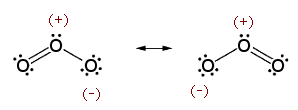
Ozon, O3, ist ein Gas, das aus drei Sauerstoffatomen besteht. Die formal 1.5-fache Bindung zwischen den Sauerstoffatomen ergibt sich aus folgenden Grenzstrukturen:
Ozon kommt in der Atmosphäre in unterschiedlichen Konzentrationen vor. Während in der Stratosphäre hohe Konzentrationen (einige ppm) erwünscht sind, um die harte UV-Strahlung der Sonne zu absorbieren, ist in bodennahen Luftschichten die Konzentration um den Faktor 100 bis 1000 geringer.
Herstellung von OzonDie Herstellung von Ozon funktioniert immer nach dem selben Prinzip: Atomarer Sauerstoff wirk auf O2 ein und bildet Ozon. Die Erzeugung atomaren Sauerstoffs kann entweder thermisch, elektrisch, mittels Licht oder chemisch erfolgen, wobei die thermische Erzeugung sehr ineffizient ist, da bei höherer Temperatur auch die Geschwindigkeit des Ozonzerfalls steigt und dadurch in Summe die Ausbeute sehr gering bleibt (<1%).
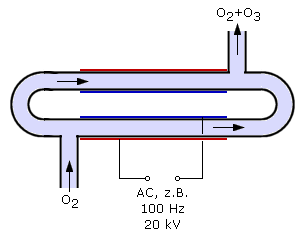
Die beste und bequemste Methode zur Erzeugung von Ozon ist die elektrische Erzeugung (Ozonisator nach Siemens). Dabei wird über eine flächige Elektrode, mit deren Hilfe an einem Rohr eine Wechselspannung mit 50 bis 500 Hz und 10 bis 20 kV Spannung angelegt wird, die benötigte Energie zugeführt. Das Rohr wird von trockenem Sauerstoff durchströmt. Die dabei ablaufende stille Entladung führt zur Bildung von Ozon (ca. 15 Vol-%), das durch fraktionierte Verflüssigung des O2/O3-Gemisches gereinigt wird. Das Rohr des Ozonisators muss gekühlt werden, da die parallel ablaufende Rückreaktion (O3 + O VerwendungHauptanwendungsgebiet von Ozon ist die Wasseraufbereitung, sowohl von Brauchwasser für die Industrie, als auch von Abwässern. Die starke Oxidationswirkung von Ozon tötet Keime im Wasser ab, oxidiert aber auch die meisten im Wasser gelösten Substanzen. Weiters wird Ozon auch zur Beseitigung von Gerüchen in Textilien eingesetzt. Hauptprobleme des Einsatzes von Ozon sind die hohen Kosten und die entstehenden Reaktionsprodukte, die oftmals nicht weniger giftig sind als die ursprünglichen im Wasser enthaltenen Substanzen. Zudem hat man mit der Chlorierung von Wasser ein deutlich billigeres Verfahren zur Entkeimung an der Hand.
|
|||||||||||||||
Home  Chalkogene Chalkogene  Sauerstoff Sauerstoff  Ozon Ozon |
|||||||||||||||
Last Update: 2013-08-08


 2 O2) sehr viel Wärme erzeugt und die Ausbeute um so besser ist, je kühler das Rohr ist.
2 O2) sehr viel Wärme erzeugt und die Ausbeute um so besser ist, je kühler das Rohr ist.